- Home
- ソリューション
- 製薬ソリューション
- Non-Clinical CRO
- 安全性評価
- 再生医療等製品の非臨床試験
再生医療等製品の非臨床試験
GLP(Good Laboratory Practice)適合施設として、再生医療等製品の非臨床試験の受託が可能です。再生医療等製品(ヒト細胞加工製品、遺伝子治療薬)の品質、非臨床試験及び臨床試験の実施に関する技術的ガイダンスに準拠し、品質評価・安全性試験を実施し、臨床試験を支援します。
ソリューション概要
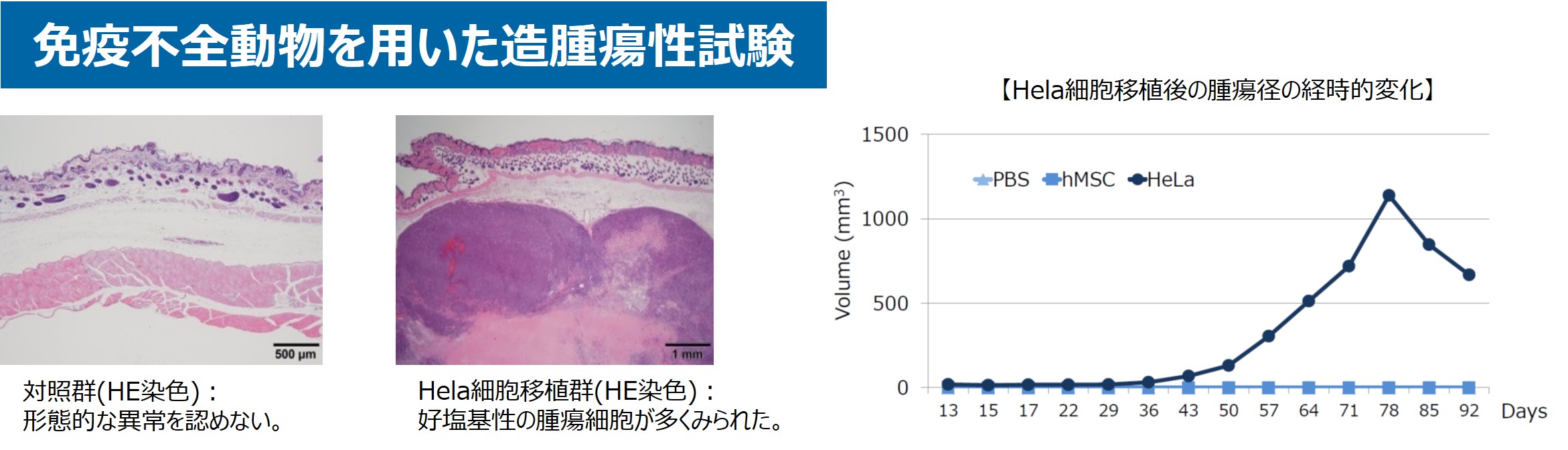
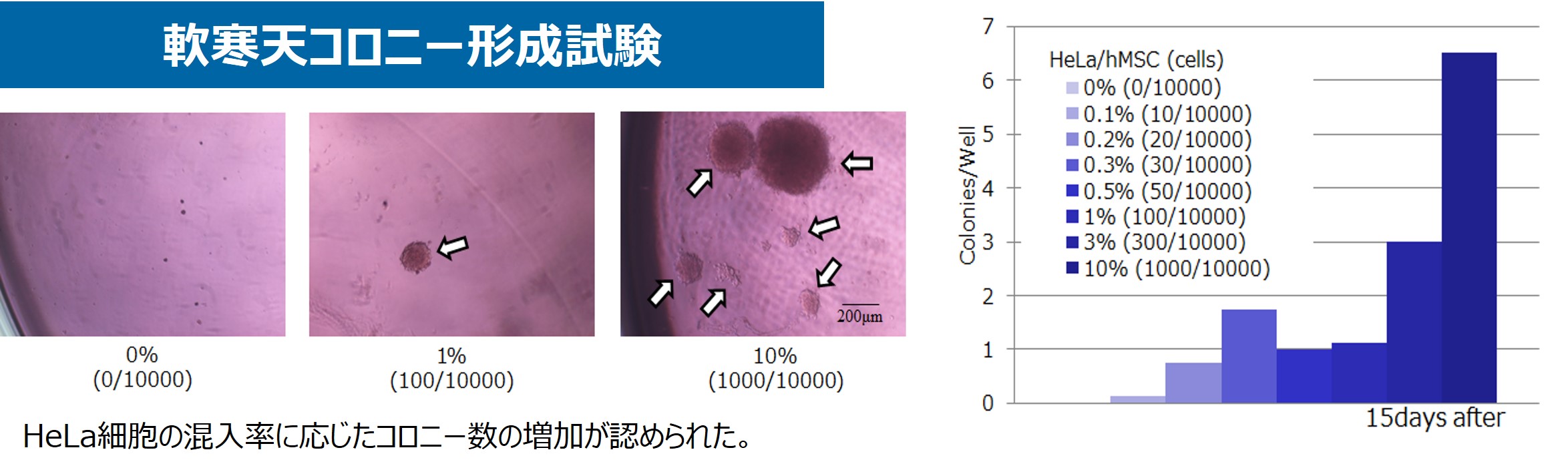
免疫不全マウスを用いた一般毒性試験、造腫瘍性試験、細胞増殖特性解析、軟寒天コロニー形成試験、体内分布試験の実施が可能です。これらの試験は、再生医療等製品の安全性および腫瘍原性評価において重要な役割を果たしています。
さらに、社内コンサルタントによる開発段階に応じた導入戦略や開発計画の立案、各種調査の実施にも対応しています。
非臨床から臨床、製造、製造販売承認取得後に至るまで、再生医療の実用化に必要なステージを包括的に支援する体制を整備しています。
ソリューションの特長
豊富な経験に基づく薬事戦略・コンサルティングと規制当局対応
再生医療等製品は製品特性が多様で、開発戦略が確立していない場合も多いため、規制当局との継続的な協議が不可欠です。シミックでは薬事戦略の立案から規制当局対応まで、再生医療等製品に関するコンサルティングを提供しています。経験豊富な専門チームが、海外企業や異業種、スタートアップを含む多様なお客さまを支援しています。
特殊な投与経路の試験支援
従来の低分子・高分子医薬品とは異なり、 再生医療等製品では、製品特性や治療対象の組織に応じて、個別に設計・開発された特殊な投与経路が求められる場合があります。医薬品の個別ニーズに対応するため、脳実質内、脳室内、髄腔内、椎間板内などの特殊経路に対応した試験系の構築と評価を行っています。
主な試験
ソリューションに関するお問い合わせ
シミックは、さまざまな課題に対し、総合力を活かした幅広いソリューションを提供しています。
課題解決に向けて、各領域のエキスパートがお客さまのお問い合わせに対応します。
資料
関連情報
- 毒性試験
- 遺伝毒性試験
- 安全性薬理試験
- 医療機器の非臨床試験
- 再生医療等製品の非臨床試験