- Home
- ソリューション
- 製薬ソリューション
- 開発領域別ソリューション
- 再生医療等製品
再生医療等製品
再生医療等製品の開発成功のカギは、適切な開発戦略や治験プロトコルの策定です。また、再生医療等製品を用いた試験では、細胞製剤やウイルスベクター製品などを扱うため、製品取り扱い上の課題や起こりうる事象を十分に理解した対応が必要です。シミックは、医薬品および再生医療等製品の開発支援を通じて得た豊富な経験と専門知識を駆使し、実用化に向けてワンストップで支援する「再生医療のトータルソリューション」を提供します。
ソリューション概要
再生医療等製品の初期開発から上市後までをシームレスにサポートします。コンサルティング、プロジェクトマネジメント、モニタリングのほか、In Country Clinical Care-taker(ICCC:治験国内管理人)としての対応も可能で、開発戦略の立案から非臨床試験、施設調査、承認申請後の監査サポートまで、幅広く対応しております。また、企業治験のみならず、医師主導治験についてもサービス提供を行っています。
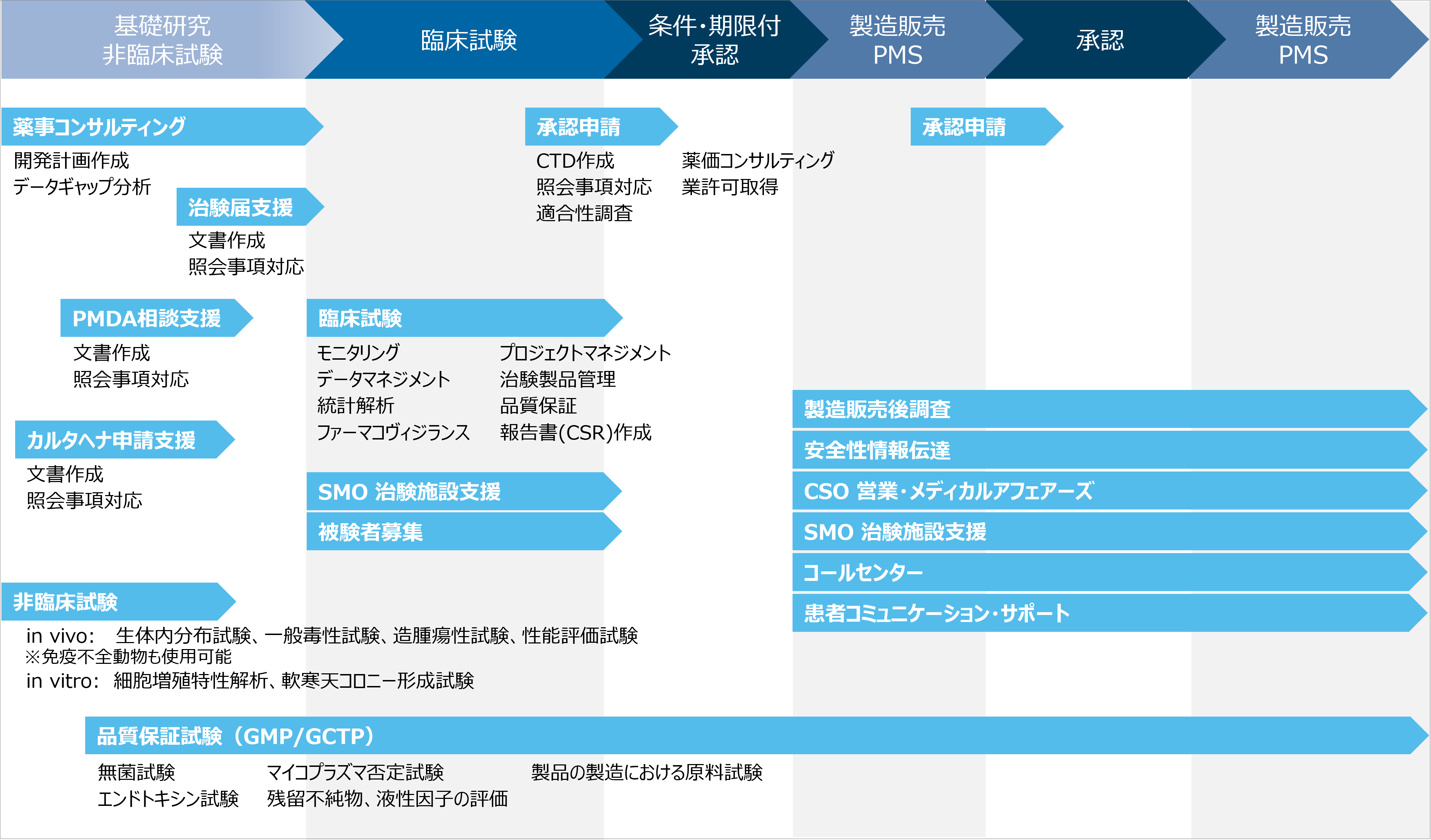
再生医療分野におけるシミックのソリューション
ソリューションの特長
再生医療分野におけるワンストップソリューション
長年の医薬品および再生医療製品の開発支援(First In Human試験を含む)で培った豊富な経験と専門知識を駆使し、開発段階に合わせた導入・開発戦略の立案や各種調査から、製造、非臨床試験、臨床試験、製造販売承認取得、市販後に至るまで、再生医療の実用化に必要なすべてのステージを支援する体制を整えています。非臨床試験の受託が可能なGLP(Good Laboratory Practice)適合施設も有しており、再生医療等製品(ヒト細胞加工製品)に関する技術的ガイダンスに準拠し、品質評価、安全性試験、臨床試験を支援します。グループ会社間の連携を活かしたワンストップソリューションによって、お客さまの開発成功率を向上、かつプロジェクトの時間とコストを大幅に削減することが可能です。
国内トップレベルの薬事戦略・コンサルティングと規制当局対応
製品特性がさまざまで開発戦略が十分に確立されていない再生医療等製品の開発は、規制当局に相談しながら進める必要があります。規制当局との相談にも戦略が必要であり、経験とノウハウが要求されます。シミックのコンサルティングチームは、非臨床段階より再生医療分野(細胞治療、遺伝子治療を含む)の薬事コンサルティングを実施しています。日本市場への参入をご検討中の海外・異業種・スタートアップ企業へのコンサルティングも含め、これまでに約130件(2024年9月末時点)と、再生医療に関する国内トップレベルの受託実績を有します。さまざまな製品のコンサルティング経験に基づき、規制当局の考え方をよく理解した上で、最適な戦略を提案します。
| 受託した製品の種類 |
|---|
|
再生医療に特化した支援
非臨床コンサルティング
高い専門性が求められる再生医療分野に対応するため、再生医療に特化した支援体制を整えています。
細胞加工製品、in vivoおよびex vivo遺伝子治療製品の非臨床コンサルティングの実績がございます。非臨床分野の国内外のガイドラインや過去の経験に基づき、開発初期から承認申請までのすべてのステージで再生医療の開発を支援します。
再生医療専門の臨床開発チーム
再生医療等製品の治験では、細胞製剤やウイルスベクター製品等を扱うため、臨床施設での製品の取り扱い上の課題や起こりうる事象を十分に理解した対応が必要です。シミックでは、幅広い製品の試験支援経験を有し製品特徴をふまえた臨床試験実施時の留意点や経験に基づいたナレッジを人財教育にも活用することで、再生医療のスペシャリストを育成しています。再生医療のスペシャリストが一丸となり、さまざまな製品の特性に応じたサポートを提供します。
ソリューションに関するお問い合わせ
シミックは、さまざまな課題に対し、総合力を活かした幅広いソリューションを提供しています。
課題解決に向けて、各領域のエキスパートがお客さまのお問い合わせに対応します。