- Home
- ソリューション
- 製薬ソリューション
- 開発領域別ソリューション
- 希少疾患(オーファンドラッグ)
希少疾患(オーファンドラッグ)
対象患者が少なく、極めて限定された治療法しかない希少疾病用医薬品(オーファンドラッグ)の開発においては、承認申請上の課題を整理し、メディカルニーズに合わせた開発戦略を策定することが重要です。また、日本政府による開発促進のための支援制度も設けられており、希少疾病用医薬品に指定された*1場合は、優先審査や医薬品の承認申請手数料減額などの対象となります。
シミックグループでは、このような優先審査制度や薬価などの出口戦略を考慮した開発戦略立案から臨床試験の実施および承認申請までのサポートのみならず、シミックグループが医薬品市販承認取得者(MAH)として流通・販売を実施するサポートも行っています。
*1:日本における希少疾病用医薬品指定の対象は、日本の患者数5万人以下の疾患
ソリューション概要
ウルトラオーファン薬*2を含むオーファンドラッグの開発・承認取得・販売に関する豊富な経験に基づき、専門的なノウハウを提供します。グループのリソースを活用し、海外企業の日本市場進出や小児疾患領域での支援にも強みを発揮しています。
*2:日本における患者数1,000人未満の疾患に対する薬剤
シミックは2015年から日本のRare Diseaseの患者活動に協賛しており、医薬品開発のみならず、患者支援という立場からも、希少・難治性疾患への取り組みを推進しています。
ソリューションの特長
グループ連携
製剤設計、臨床開発の計画、試験の実施、製造販売承認申請、薬価戦略におけるコンサルティングなどの幅広い分野のスペシャリストが在籍しており、医薬品開発に必要なすべての機能が揃っています。お客さまのニーズに応じて必要なサービスを組み合わせ、グループ内で密に連携し、よりよい薬をより早く患者さんのもとへお届けできるようサポートします。
希少疾患治療薬開発および申請における豊富な経験
小児先天性疾患領域をはじめ、各疾患領域のKey Opinion Leader(KOL)や医療機関とのネットワークも活用しながら、経験豊富な担当者が開発戦略を提案し、日本の規制当局との開発相談を調整するとともに、希少疾病用医薬品指定申請から治験実施、製造販売承認申請、グループ内の製薬会社であるオーファンパシフィックによる製造販売まで、患者さんへお薬を一日でも早く届けられるようサポートします。また、海外の製薬企業に対し、日本における製薬企業の立ち上げ支援も行っています。
安定供給のノウハウに基づくサプライチェーンマネジメント
ウルトラオーファンを含む、希少疾病用医薬品の製造と流通においては、患者数が少なく製造量が少ないために、品質管理や、必要なタイミングで医療機関や患者さんの元へ製品を確実に届けるためのノウハウが必要です。シミックグループでは、これまでの希少疾患治療薬の製造、流通におけるノウハウと経験に基づくバリューチェーンを活用したサプライチェーンマネジメントにより安定供給を目指します。
実績
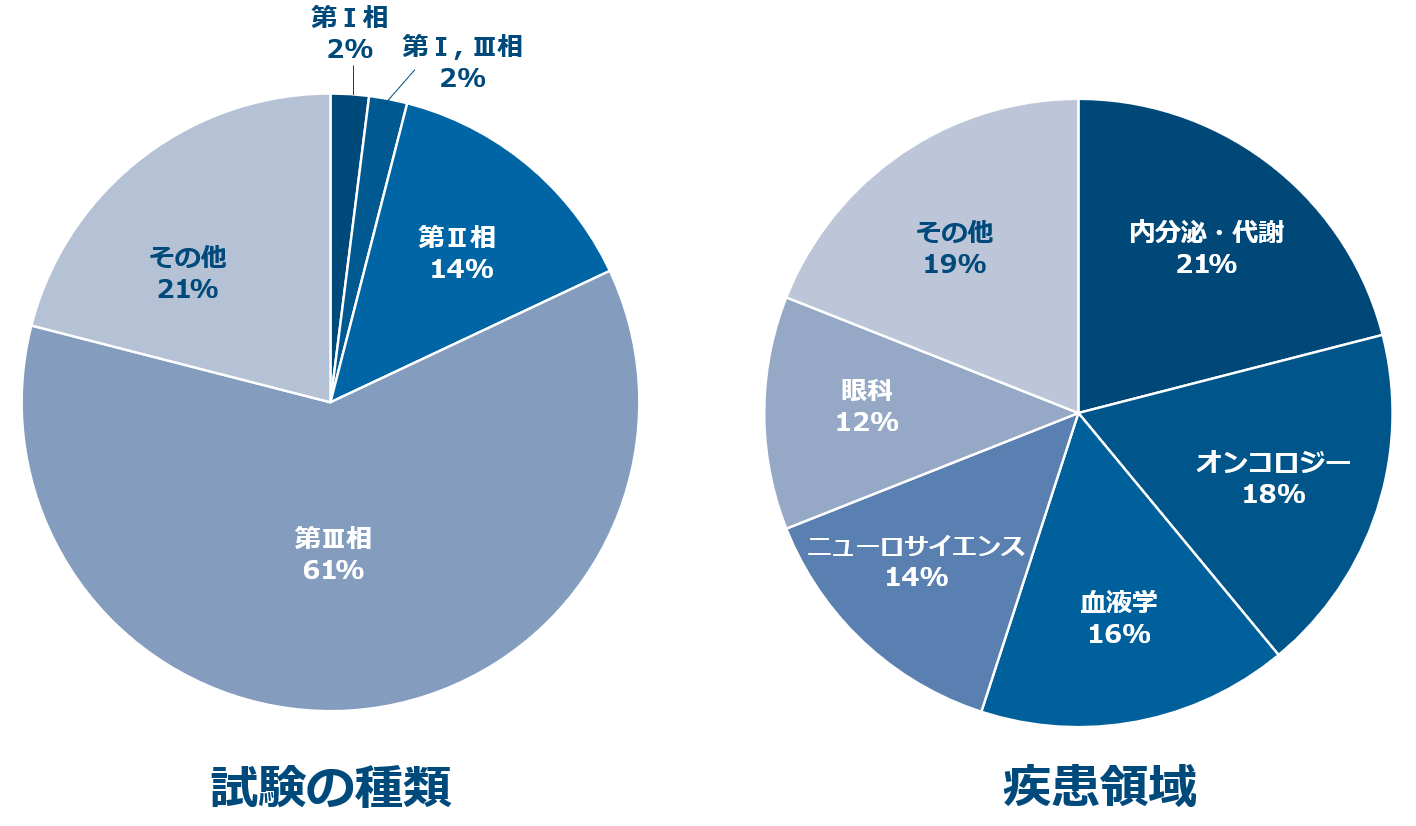
シミックはこれまで多くの希少疾患の試験(下図参照)に携わっており、Medical Needsの高い希少疾患患者に新たな治療薬等を提供できるよう支援しております。ウルトラオーファン薬のグローバル試験において、日本の目標症例数を上回る登録実績や、その他専門医と連携した活動などの事例に基づき、円滑に臨床試験を進めるご提案をします。
ソリューションに関するお問い合わせ
シミックは、さまざまな課題に対し、総合力を活かした幅広いソリューションを提供しています
課題解決に向けて、各領域のエキスパートがお客さまのお問い合わせに対応します。
資料
関連情報
- オンコロジー
- ニューロサイエンス
- 医療機器・体外診断用医薬品
- 希少疾患(オーファンドラッグ)
- 再生医療等製品