- Home
- ソリューション
- 製薬ソリューション
- 開発領域別ソリューション
- 医療機器・体外診断用医薬品
医療機器・体外診断用医薬品
近年、医療機器開発は技術革新により複雑化/多様化し、薬事規制や臨床試験の要件も高度化しています。こうした課題に対し、シミックの医療機器本部は、技術の発展に合わせた医療機器開発の課題に対して、的確かつ柔軟に対応できる医療機器開発のエキスパート集団です。医療機器および体外診断用医薬品のすべての開発フェーズにおいてトータルソリューションを提供します。
ソリューション概要
シミックの医療機器本部は、医療機器全般(SaMD含む)と体外診断用医薬品においても豊富な経験を持つ医療機器開発のエキスパート集団です。これまでに培った豊富な知識とノウハウを活かし、日本発の医療機器開発のみならず、海外から日本市場への参入や異業種からの参入を支援します。
医療機器に特化した薬事コンサルティングと臨床開発を専門とするグループで体制構築しているため、薬事戦略、臨床試験から薬事承認そして市販後調査に至るまで、一貫して最良のソリューションを提供します。
ソリューションの特長
ワンストップ伴走型コンサルティング
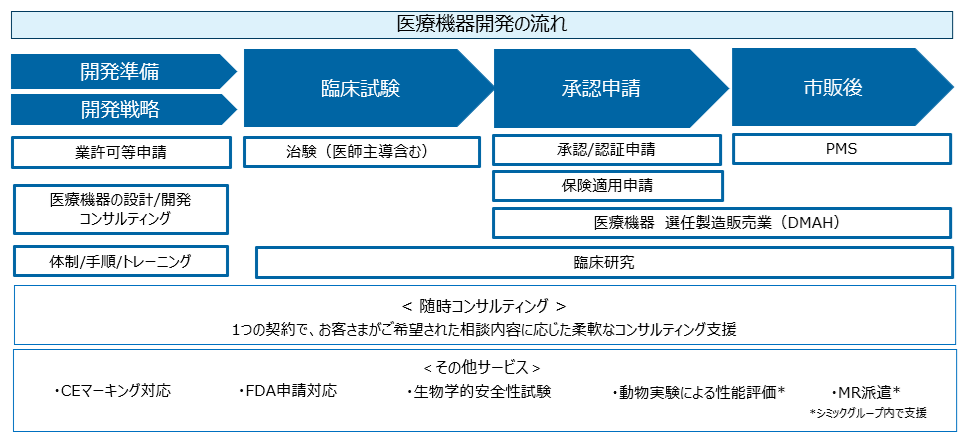
お客さまの多種多様なニーズに応じた戦略と対応すべき課題を包括的に検討し、部分的な業務委託に関するご相談に限らず、事業や製品の企画から戦略作成、体制構築、許可取得、保険適用、市販後の対応に至るまで、これらの煩雑なプロセスをお客さまとゴールを共有しながら伴走し、一貫した支援を実現します。
| 業許可等申請 | 設計/開発 コンサルティング |
|---|---|
| ・許認可申請 ・QMS省令対応・ISO13485/MDSAP認証取得支援 |
・薬事・開発戦略 |
| 体制/手順/トレーニング支援 | 保険適用申請 |
|
・実施体制の構築
・手順の整備
・セミナー、講習会の実施
|
・保険適用希望書の作成 ・規制当局との折衝 |
| 承認/認証申請 | 選任製造販売 |
| ・薬事戦略立案 ・申請資料作成・提出・照会対応 ・QMS適合性調査対応 ・製造業登録・製造販売業取得支援 |
・医療機器 選任製造販売業者 |
| FDA申請対応 | CEマーキング対応 |
| ・510(K)申請 ・QSMR対応 |
・欧州医療機器規則(MDR)申請対応欧州体外診断医療機器規則(IVDR)申請対応 ・技術文書の作成 ・臨床評価 |
医療機器臨床試験のトータルソリューション
~治験・臨床研究・市販後調査(PMS)の全てに対応~
豊富な実績とあらゆる臨床試験ニーズに応える専門チームとして、以下に示すような各規制に基づく臨床試験の企画段階~臨床試験~研究報告書の作成までの全業務におけるソリューションを提供しています。加えて、心血管領域、整形外科領域、眼科領域、神経内科領域、脳神経外科領域、プログラム医療機器、体外診断薬など、あらゆる品目の開発経験を有しています。
- 人を対象とする生命科学・医学系研究に関する倫理指針
- 臨床研究法
- 医療機器の臨床試験の実施の基準に関する省令(医療機器GCP):企業主導・医師主導治験
- 医療機器の製造販売後の調査及び試験の実施の基準に関する省令(GPSP):医療機器PMS
治験(医師主導治験含む)
| 治験(医師主導治験含む) |
|---|
|
臨床研究・特定臨床研究
| 臨床研究・特定臨床研究 |
|---|
|
医療機器PMS
| 医療機器PMS |
|---|
|
分野横断的な製品開発コンサルティング
医薬品や再生医療等製品のコンサルタントと、医療機器本部とのコラボレーションによって、コンビネーション製品やコンパニオン診断薬など、同時開発を必要とする製品においても、規制要件の整理から、戦略的な開発計画の立案、申請支援に至るまで、各分野の専門知識を融合させることで、複雑な開発課題にも多角的に対応いたします。
実績
医療機器コンサルティンググループの実績
医療機器 - 主な製品 -
| 医療機器 - 主な製品 - | |
|---|---|
|
|
体外診断用医薬品
| 体外診断用医薬品 |
|---|
|
医療機器・体外診断用医薬品開発などの臨床試験に関する実績
主な疾患領域
| 主な疾患領域 | |
|---|---|
|
|
ソリューションに関するお問い合わせ
シミックは、さまざまな課題に対し、総合力を活かした幅広いソリューションを提供しています。
課題解決に向けて、各領域のエキスパートがお客さまのお問い合わせに対応します。
関連情報
- オンコロジー
- ニューロサイエンス
- 医療機器・体外診断用医薬品
- 希少疾患(オーファンドラッグ)
- 再生医療等製品