治験から臨床研究まで、幅広くサポート
 シミックグループは、日本で初めてSMO(Site Management Organization:治験施設支援)業務を事業化しました。業界のパイオニアとしての豊富な実績とともに、高度なノウハウを活かして、治験実施体制の整備支援から実施・運営までの事務・実務をトータルにサポートしています。また、医療機関との事業連携の強みを生かし、ヘルスケア分野への新規事業の展開を図っています。
シミックグループは、日本で初めてSMO(Site Management Organization:治験施設支援)業務を事業化しました。業界のパイオニアとしての豊富な実績とともに、高度なノウハウを活かして、治験実施体制の整備支援から実施・運営までの事務・実務をトータルにサポートしています。また、医療機関との事業連携の強みを生かし、ヘルスケア分野への新規事業の展開を図っています。
シミックのSMOの強み
すべての疾患領域をカバーするノウハウと実績、 大規模病院からクリニックまで全国の医療機関と提携
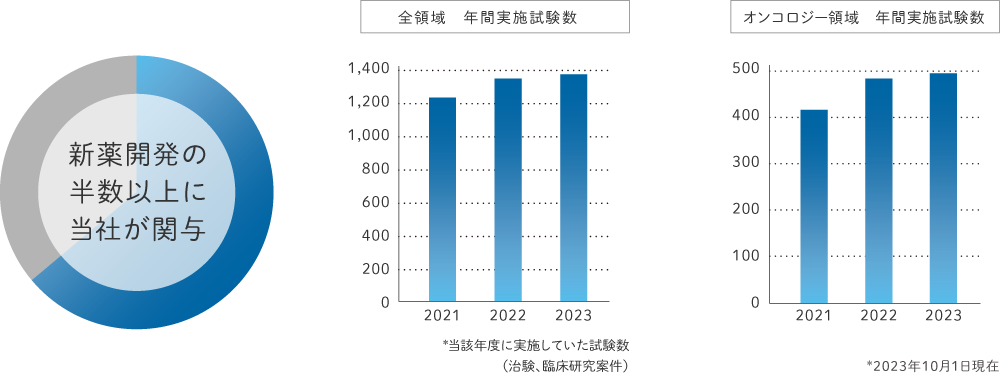
- 直近5年のプロトコール実績:約1,770プロトコール(2018年10月~2023年9月)
オンコロジー、中枢神経、自己免疫領域など幅広い領域の試験に対応しています。
- 治験実施医療機関数:約4,000(2023年10月現在)
北海道から九州、沖縄まで、全国の各エリアの医療施設と提携し、治験依頼者へポテンシャルの高い実施候補医療機関の紹介が可能です。
全国の主要都市に拠点を展開し、効率的且つ質の高い治験支援業務を実施
- 国内全域をカバーする拠点数:26拠点
- 専門領域および倫理的研修を受けたプロフェッショナルなスタッフ
がん研修、中枢疾患研修など、 開発トレンドに応じた専門研修を実施
臨床研究・医療における倫理的・法的・社会的課題(ELSI*)に関する研修を実施
*Ethical, Legal and Social Issues
- プロジェクトマネジメント体制
複数の地域におよぶ大規模プロジェクトでは、プロジェクトマネジメント部門が全体を統括し、情報統制を含め、効率的かつスピーディーに試験を進行するよう調整しています。
- クオリティマネジメント
担当CRC・SMAによる品質維持を目的とした日々の業務チェックはもちろんのこと、QC担当者がプロセス管理や医療機関でのQC点検を行うことで、試験全体の高品質確保に努めています。
臨床研究支援業務(CSS:Clinical Study Solution)
臨床研究の計画から論文公表、またCRCによる医療機関サポートまで、臨床研究を総合的に支援しています。
- 研究事務局業務
臨床研究の企画・立案から実施、終了まで、研究者および製薬企業・CROを幅広く支援可能なスタディマネジメント機能を提供
- 倫理審査委員会
- モニタリング業務(On-Site, Off-Site Monitoring対応)
臨床研究モニタリング教育プログラムで学び、独自の認定制度に基づきモニター認定を受けた当社の担当者が全国拠点で活躍しており、様々な規模の臨床研究を支援
- 監査業務
- 医療機関支援
サービス実績
オンコロジー、中枢神経、自己免疫の領域など、ライフサイエンスの進歩により、今までになかった新たなアプローチで新薬が創出されるようになりました。当然、これらの新薬を世の中に送り出すための臨床試験でも、最先端のライフサイエンスの知識とノウハウが必要になってきます。当社はこの新たな領域でも、近年多くの実績を有しています。
年間約1,400もの試験を全国各地で支援し、オンコロジー領域における支援は年間約500試験となります。
主なサービス内容
治験開始前
- 治験業務フローの作成
- 症例管理のための資料作成
- 実施計画書に伴う研修
- 治験関連部門との連絡・調整
被験者対応
- 同意説明の補助
- 被験者適格性確認
- 被験者の相談窓口
- 緊急時の対応窓口
- 診察・検査立ち会い
- 被験者のスケジュール管理
- 服薬状況の確認(残薬の回収、返却)
- 併用薬・有害事象確認
- コンプライアンス確認
- 保険外併用療養費請求業務の支援
治験担当医師対応
- 同意説明の補助
- 同意説明書の作成支援
- スクリーニング作業の補助
- 治験実施計画書遵守の補助
- 症例報告書作成の補助
- 被験者適格性調査の補助
- 有害事象対応支援
- 安全性に関する確認補助
治験関連部門との連絡・調整
- 協力者会議開催
- 各部門への説明会開催
- 薬剤部(治験薬概要、オーダリング業務)
- 検査部・看護部・医事課
- 治験薬搬入・回収の補助
依頼者対応
- 医療機関・治験責任医師適格性調査対応
- 治験実施状況の報告
- モニタリング・SDV・監査時対応
- 症例報告書のフィードバック時などの窓口
- 直接閲覧の対応
- メーカー監査・実地調査への対応
医療機関での治験を開始するための補助
- 施設SOPの作成・提供
- GCP対応書式の提供
- 治験責任医師/分担医師、治験協力者の教育
医療機関での治験を実施するための補助
- 治験事務局の立ち上げ
- 治験事務局の運営補助
- 治験事務局の教育
IRBの設立・運営の補助
- IRBのSOPの作成・提供
- IRB委員、IRB事務局の教育
- IRBの運営補助
- IRB事務局補助(議事録、審査結果報告書などの作成)
CRC(治験コーディネーター)の教育と支援体制
- CRCの教育研修
- CRC業務のフォロー
- バックアップ体制の確保

SHARE